enzimatikus analízis
Az enzimek fontos szerepet játszanak a biokémiai vizsgálatok. A biológiai anyagok, mint például a testfolyadékok, meghatározzuk a katalitikus enzimek aktivitása is kimutatható nagyon kis koncentrációban is. Enzimek lehet használni, mint reagensek koncentrációinak meghatározására metabolitok, mint például a vér glükóz (B reakcióvázlat). A legtöbb enzimatikus vizsgálatok használt fotometriával.
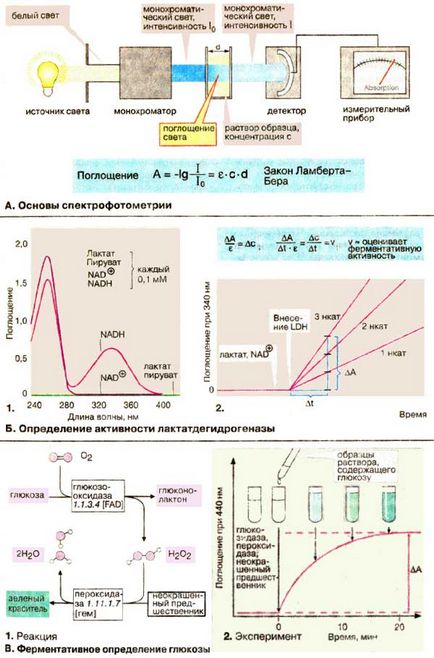
A. alapjai spektrofotometriás
Sok molekulák elnyelik a látható fény vagy ultraibolya tartományában a spektrum. Ez a tulajdonság lehet használni, hogy meghatározzuk a koncentrációt. Az abszorpciós típusától függ, és az anyag koncentrációja, valamint a fény hullámhossza használt. Ezért a monokromatikus fény használni. t. e. fényt egy bizonyos hullámhosszon, amely izolálható fehér fény alkalmazásával monokromátor. Monokromatikus fény intenzitása I0 áthalad a téglalap alakú cella üvegből vagy kvarcból (küvetta), amelyben az abszorbens anyag van megoldás. Az I intenzitását a kialakuló fény, károsodott abszorpciót mérjük egy detektorral. Fényelnyelési (A) Az oldat (optikai sűrűség) határozza meg, mint a negatív logaritmusa arányának I / I0. Act Lambert-Beer kimondja, hogy a arányos a koncentráció (k) az anyag és a vastagsága (d) az oldat réteg. kioltási együttható # 949; függ, mint fentebb megjegyeztük, az anyag típusa és a hullámhossz.
B. meghatározása laktát-dehidrogenáz aktivitás
Meghatározása laktát-dehidrogenáz [LDH (LDH)] azon a tényen alapul, hogy a csökkent koenzim NADH + H + fényt abszorbeál 340 nm-en, míg a NAD + (NAD +) ezen a hullámhosszon nincs felszívódás. Az abszorpciós spektrumokat (m. E. A grafikus függően hullámhosszon) a hordozó és a koenzimet LDH reakcióban ábrán látható. B1.
Különbségek a felszívódását a NAD + és a NADH közötti 300 és 400 nm-en bekövetkező változások miatt a nikotinamid gyűrűt a oxidáció vagy redukció (lásd. P. 102). Ahhoz, hogy meghatározzuk a aktivitást a küvettát elsődlegesen oldatok laktát és NAD +, és az abszorbanciát rögzítjük állandó 340 nm hullámhosszon. Nem-katalitikus reakció egy nagyon kis sebességgel. Ezért a mért NADH alakult csak hozzáadása után a LDH. Mivel a növekedés mértéke az abszorbancia # 916; A / # 916; t a Beer-Lambert törvény arányos a reakció sebessége # 916; c / # 916; t. LDH-aktivitás lehet kiszámítani extinkciós koefficienst használva # 949; 340 nm-en, vagy összehasonlítva a standard oldatot.
B. enzimatikus meghatározása glükóz
A legtöbb biomolekulák nem nyelik el a fényt a látható és ultraibolya tartományában a spektrum. Továbbá, ezek általában jelen keverékben más vegyületek, amelyek szintén adnak hasonló kémiai reakciók. Mindkét probléma lehet leküzdeni a megfelelő enzim szelektív átalakítás határozzuk metabolit egy színes anyagot, melyet tovább által meghatározott fényelnyelés intenzitása.
A szokásos módszerrel történő meghatározásának a vér glükóz (.. 162 cm), amely két, egymást követő reakciók:
1) a kialakulását glukono-laktont és hidrogén-peroxid H2 O2, az enzim által a glükóz-oxidáz;
2) oxidációja színtelen anyag hidrogén-peroxid a zöld színű vegyület által katalizált reakció peroxidáz.
Amikor az összes rendelkezésre álló glükóz a mintában használjuk fel, az összeg a színes anyagok képződött lehet meghatározni fényelnyelés, amely egyenesen arányos az eredeti glükóz-tartalmat.