Salt - osztályozására, előállítása és tulajdonságai
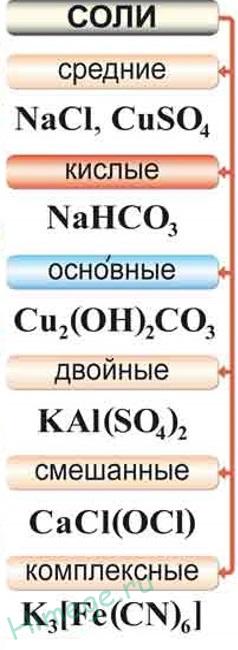
Sókat tartalmazó táptalajban nevű termékek teljes csere hidrogénatomok a molekulában, a savas fém-atomok, vagy teljes helyettesítése bázisok a molekulában gidroksogrupp-maradékok.
Például, H3 PO4 - Na3 PO4;
Cu (OH) 2 - CuSO 4.
Acid sókat nevezzük a tökéletlen szubsztitúció a hidrogénatomok a molekulák a fématomok több-bázisú savak.
Például, a H2 SO4 - NaHSO 4,
H3 PO4 - Na 2HPO 4 - NaH 2PO 4.
Bázikus sókat nevezzük a tökéletlen szubsztitúciós gidroksogrupp mnogokislotnyh bázisok savas maradékok.
Például, Ca (OH) 2 - CaOHCl;
Fe (OH) 3 - Fe (OH) 2 Cl - FeOHCl2.
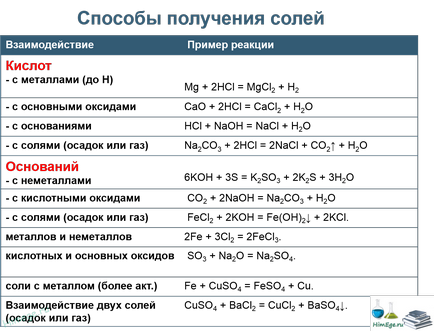
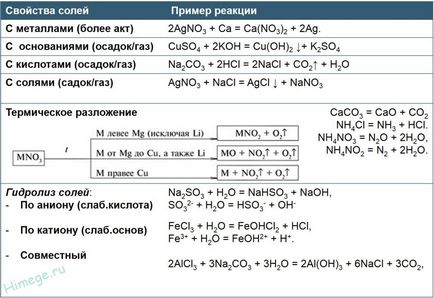
A savas sók reagálnak lúggal só táptalajt.
KHCO3 + KOH = K2 CO3 + H2 O
Néhány savas sók, például, szénsav elbomlik hatására erősebb savak:
KHCO3 + HCl = KCl + CO2 + H 2O
Bázisos sókat egy savval kezeljük:
Cu (OH) CI + HCI = CuCI 2 + H2 O
A tulajdonságok a komplex sók (komplex sók módszerek törés)
1) komplex sóit reagálnak erős savakkal, a reakció termékek függ közötti arány a reaktánsok. Az intézkedés alapján egy feleslegben lévő erős savval kapott két magas só és víz. Az akció a hiánya erős savat kapunk átlagos fémsó hatóanyagot, egy amfoter-hidroxiddal és vízzel, például:
2) A fűtési komplex sók elveszítik a víz:
3) Amikor az intézkedés a szén-dioxid, kén-dioxid vagy a hidrogén-szulfid előállított só és az amfoter aktív fém-hidroxid:
4) Amikor az intézkedés a sók kationokkal Fe 3+. Al 3+ és Cr 3+ kölcsönös erősödése hidrolízis kapott két amfoter hidroxidot és aktív fémsó: